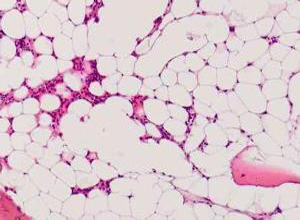
阵发性睡眠性血红蛋白尿症(paroxysmal nocturnal hemoglobinuria,PNH)是一种后天获得性造血干细胞基因突变导致红细胞膜病变而引起的慢性溶血性疾病,临床上以间歇发作的血管内溶血、血红蛋白尿,睡眠后溶血加重为特点。男女均可发病,男性较多,多见于青壮年,小儿时期极少见。
-
挂什么科:儿科 儿科综合
-
需做检查:核糖核酸染色 尿常规 尿隐血(BLD) 碱性磷酸酶染色 骨髓象分析 铁染色 蛇毒因子溶血试验 酸溶血试验 血常规 便常规 血管造影 CT检查
-
治疗方法:药物治疗 支持性治疗
-
常用药物:暂无相关信息
-
一般费用:根据不同医院,收费标准不一致,市三甲医院约﹝10000--30000元﹞
-
传染性:无传染性
-
治愈周期:1-3个月
-
治愈率:30%
-
患病比例:0.0001%
-
好发人群:儿童
-
相关症状:
-
相关疾病:
起病缓慢,首发症状为轻重不等的贫血,多数病人有血红蛋白尿,其尿呈酱油色或棕色,但有25%病人在病程中始终无血红蛋白尿,血红蛋白尿多在夜间睡眠后发生,清晨睡醒时较重,下午较轻,白天睡眠也可致发作,发作时常伴有寒战,发热,头痛,腹痛,腰痛等症状,血红蛋白尿的发作情况差别很大,有的仅偶然发作,有的发作频繁,并常伴有黄疸,发作的诱因以感染为多见,药物,输血反应,疲劳和手术等均可诱发,溶血的量与许多因素有关:
1.异常克隆的大小 血液循环中补体敏感红细胞的所占比率差异很大,1%~90%,这些细胞都有发生溶血的危险。
2.红细胞的异常程度 差异也很大,这与细胞膜表面补体防御蛋白的含量差异较大有关。
3.补体活化的程度 感染,输血反应等均可引起补体活化,特征性的睡眠性溶血可能是由于内毒素经肠道吸收而致补体活化有关,长期血红蛋白尿可引起肾内含铁血黄素沉着,而致含铁血黄素尿,长期的血红蛋白尿和含铁血黄素尿又可使体内铁丢失,而致缺铁性贫血,有些病人由于血小板的减少及其功能异常,而有出血倾向,如齿龈出血,鼻出血和皮肤出血等,血红蛋白尿频繁发作者,由于长期红细胞破坏过多或输血过多可致轻度黄疸或皮肤色素沉着,肝脾常轻度肿大,有些病人在病程中可出现再生障碍性贫血的临床表现,少数病人可转变为急性白血病或骨髓纤维化。
(一)发病原因
目前认为,PNH的病因在于后天获得性造血干细胞基因突变,PNH病人外周血中,正常和异常红细胞,粒细胞,单核细胞和血小板同时存在,提示异常细胞起源于骨髓中的一个克隆,早有研究发现,有G6PD变异的女性杂合子病人可见到异常的PNH红细胞均具有一个同工酶,该酶基因位于X染色体上,因而推测,这些异常细胞起源于具有上述同工酶的单一祖细胞,这一发现及近年来的大量研究均有力支持异常细胞群起源于单一祖细胞的观点,导致造血干细胞发生基因突变的确切原因尚不清楚,临床上PNH与再生障碍性贫血可相互转化或同时存在,因而推测可能的发病机制是:某种致突变源使造血干细胞发生突变,加上病毒,某些药物等因素导致免疫功能失调,使正常的造血干细胞受损而减少,突变的造血干细胞有机会增殖而发病,这一学说尚需研究证实,
(二)发病机制
1.病理生理 PNH的病理生理主要与细胞膜表面缺乏一组糖肌醇磷脂(GPI)连接蛋白有关;而GPI连接蛋白的缺乏又继发于GPI锚合成缺陷,
(1)GPI锚合成缺陷:几乎所有PNH病人都有pig/α基因(定位于Xp22)异常,该基因缺陷可引起N-乙酰葡萄糖胺不能加到磷脂酰肌醇上,因而最终不能形成完整的GPI锚,
(2)GPI连接蛋白缺陷:目前发现,PNH病人异常细胞上至少有15种蛋白质发生不同程度的缺乏,此与异常细胞的功能有着密切关系,此类蛋白质可分为补体防御蛋白,免疫分子,酶类,受体类及功能未知的粒细胞蛋白质类等,
2.发病机制 目前认为,PNH病人的红细胞对补体的溶血作用敏感性增强的主要原因是细胞膜缺乏CD55和CD59两种膜蛋白,从而导致对膜表面补体活化的调控作用减弱,CD55又称衰变加速因子(decay accelerating factor,DAF),能增加转化酶复合物解离或衰变的速度,异常PNH细胞膜上CD55的缺乏使转化酶活性增高,因此导致更多的C3沉积于膜上,CD59又称反应性溶血膜抑制物(membrane inhibitor of reactive lysis,MIRL),能抑制补体活化过程中C8和C9之间的相互作用,PNH红细胞上的CD59缺乏可导致红细胞对补体溶血作用的敏感性增强;但PNH异常血小板上的CD59缺乏并不导致血小板破坏,而主要在PNH并发静脉血栓形成中起作用,因为PNH血小板上多聚C9复合物的形成调节障碍,所以有更多的C9复合物插入膜中,产生更多的血栓素,而PNH的异常血小板又对血栓素的反应特别敏感,所以PNH病人易于并发血栓形成, PNH病人粒细胞上Fcγ受体Ⅲα(CDl6a)缺乏可以使病人易于感染,特别是血源性感染,乙酰胆碱酯酶活性降低是本病特征之一,PNH红细胞乙酰胆碱酯酶活性降低程度与病情轻重相平行,目前认为,该酶活性降低可能继发于红细胞膜脂质异常,与溶血的发生无关,PNH细胞其他蛋白质,如CD58,CD14,CDw52,乙酰胆碱酯酶,白细胞碱性磷酸酶,尿激酶受体,叶酸受体等丢失的意义不明, 3.PNH红细胞分为3种 根据红细胞对补体溶血的敏感性的不同,可将PNH红细胞分为3种:
(1)极敏感红细胞:它对补体溶血的敏感性为正常红细胞的25~30倍,
(2)中度敏感红细胞:它对补体的敏感性较正常红细胞高3~5倍,
(3)正常红细胞,临床上,约78%PNK病人同时存在(1)和(3)两种细胞,约9%同时存在(1)和(2)两种细胞,其余病人同时存在(2)及(3)两种细胞,极少数病人只有(2)细胞,临床表现的严重程度与(1)细胞群所占比例的多少有关,一般情况下,当(1)细胞占20%~50%时即可发生血红蛋白尿,但(2)细胞所占比例虽然高,其临床表现则大多较轻,可不出现血红蛋白尿,此外,一些病人的敏感红细胞所占比例可以随病情发展而改变;有的病人经数月或数年后,敏感红细胞所占比例减少,病情也随之减轻或缓解,
4.诱发溶血因素 本病在睡眠时病情加重,其原因未明,目前认为可能因睡眠时血流缓慢,组织和器官内酸度升高,使血液趋于酸性而致溶血,此外,感染,特别是病毒性感染,药物(如阿司匹林,氯丙嗪,氯化铵,呋喃坦啶,铁剂等),输血,手术,劳累,精神创伤等均可诱发溶血。
诊断
根据溶血性贫血的临床表现,血红蛋白尿和酸溶血试验阳性,即可确诊,对于表现为增生低下性贫血而溶血的证据不明显者,需追踪观察才能明确诊断,我国目前制定的PNH诊断标准及再障-PNH综合征的诊断标准如下。
1.PNH诊断标准
(1)临床表现:符合PNH。
(2)实验室检查:Ham试验,糖水试验,蛇毒因子溶血试验,尿潜血(或尿含铁血黄素)等项实验中凡符合下述任何一种情况,即可诊断:
①两项以上阳性。
②一项阳性,但须具备下列条件:两次以上阳性,或1次阳性,但操作正规有阴性对照,结果可靠,即时重复仍阳性者;有溶血的其他直接或间接证据,有肯定的血红蛋白尿出现;能除外其他溶血特别是遗传性球形红细胞增多症,自身免疫性溶血性贫血,葡萄糖-6-磷酸脱氢酶(G-6-PD)缺乏症和阵发性冷性血红蛋白尿症等。
2.再障-PNH综合征诊断标准 凡再障转化为PNH,或PNH转化为再障,或兼有两病特征者,均属再障-PNH综合征,为表明两病发生先后,或兼有两病特征时,临床表现以何者为主,可将本综合征再分为4种情况,能分辨者应予标明:
(1)再障-PNH:指原有肯定有再障(而非未能诊断的PNH早期表现),转为可确定的PNH,再障的表现已不明显。
(2)PNH-再障:指原有肯定的PNH(而非下述的第4类),转为明确的再障,PNH的表现已不明显。
(3)PNH伴有再障特征:指临床及实验室检查所见均说明病情仍以PNH为主但伴有1个或1个以上部位骨髓增生低下,巨核细胞,网织红细胞不增高等再障表现者。
(4)再障伴有PNH特征:只临床及实验室检查所见均说明病情人以再障为主,但伴有PNH的有关化验结果阳性者。
鉴别诊断
本病应与再生障碍性贫血,自身免疫性贫血,骨髓增生异常综合征(MDS),营养性巨幼细胞性贫血和其他原因所致的血红蛋白尿鉴别,一般根据上述各病的临床和实验室检查特点不难作出鉴别,如果再障病人骨髓增生低下,而又能查出类似PNH的异常红细胞,或有PNH临床表现和实验室检查所见而骨髓增生低下者,应怀疑再障-PNH综合征,一些MDS病人也可出现类似PNH的异常血细胞,但其基本特点和病情的发展仍以MDS为主,很少发生典型血红蛋白尿或出现PNH表现。
小儿阵发性睡眠性血红蛋白尿症西医治疗
常规治疗主要是控制溶血发作,如右旋糖酐、碳酸氢钠、肾上腺皮质激素等免疫抑制剂,以及雄激素刺激血细胞生成。长期血红蛋白尿可导致缺铁。铁剂可使活性氧产生,PNH细胞对氧化损伤很敏感,易诱发血红蛋白尿。肯定缺铁后应从小剂量开始治疗,为常规剂量的1/3~1/10,仍有反应者应停用。输血除能提高血红蛋白,维持组织需氧,尚能抑制红细胞生成,间接减少补体敏感的红细胞。近来,PNH治疗主要有以下进展:
Eulizumab
Eculizumab人源型抗补体C5单克隆抗体,补体C5是补体级联反应中最后一个酶促反应底物,C5在C5转化酶作用下裂解为C5a和C5b, C5b参与膜攻击复合物(MAC)C5b-9的形成。Eculizumab是抑制末端补体成分活化的重组人源型单克隆抗体,能特异性与人末端补体蛋白C5结合,通过抑制补体C5向C5a和C5b的裂解,阻断炎症因子C5a的释放及膜攻击复合物C5b-9的组成。临床研究
表明,该抗体对C5有高度亲和力,能阻断C5a和C5b-9的形成,并保护哺乳动物细胞不受C5b-9介导的损伤,完全阻断补体介导的血细胞破坏。
Eulizumab可以降低PNH患者血压,从而改善患者肺动脉高压的情况。有文献报道,大部分PNH患者血NT-proBNP水平较高,它是肺血管阻力增加、右心室舒张功能不全的标志,最终会导致PH 的发生。用Eulizumab治疗后,溶血、NO清除、血管张力、呼吸困难等症状在2周内会得到明显改善,同时高NT-proBNP水平也有所下降。可以认为PH的改善是由于溶血、NO消耗、肺血管阻力的快速下降,或者肺微血栓的迅速溶解的结果。在Eulizumab治疗1-4周过程中,患者的血压明显下降,收缩压中位改变为-10mmHg。已经发现患者NT-proBNP高水平、呼吸困难与肺动静脉压力升高高度相关。
Eulizumab还能够使患者呼吸困难的症状得到改善。呼吸困难是肺压力增高的重要表现。Anita Hill等观察了Eulizumab对呼吸困难治疗的疗效,与安慰剂组相比实验组患者呼吸困难明显改善(P<0.001),大概2周左右出现疗效,持续到实验结束。值得注意的是患者呼吸困难的改善与血浆游离血红蛋白的水平无关。血红蛋白总水平在Eulizumab 26周的治疗过程中并没有发生改变。
Eulizumab能够减少血栓的形成。血栓形成是PNH患者最常见的症状,肺栓塞及肺微血栓形成也可以导致肺动脉高压。为了确定Eulizumab对血栓形成的影响,Peter Hillmen等对195例患者进行了对照试验,接受Eulizumab治疗的患者血栓发生率从7.37%降至1.07%(P<0.01),而未接受Eulizumab治疗的对照组血栓发生率从2.34%升至4.38%;接受抗凝治疗的血栓发生率为10.61%,同样的病人再接受Eulizumab治疗血栓的发生率降至0.62%(P<0.01)。说明抗凝治疗不足以预防血栓的形成,而Eulizumab可显著减少PNH病人血栓的发生率。
Eulizumab减少补体介导的溶血作用,使红细胞的破坏减少,溶血依赖的输血就会相应减少,从而提高患者的生活质量。
联合化疗
对于难治、复发的PNH患者还可以进行联合化疗。有文献报道,予8例难治及复发的PNH患者化疗方法,其中3例应用DA方案:柔红霉素40mg静滴,第1、2天,20mg静滴,第3天,阿糖胞苷100mg/d静滴,共5天。5例使用HA方案:高三尖杉酯碱2-3mg/d静滴,共5天;阿糖胞苷100mg/d静滴,共5天。同时给予基础及支持治疗。结果发现8例例患者化疗均有效。治疗后所有患者肾上腺糖皮质激素的用量较化疗前减少66%-100%,中位数75%;化疗前用量为(62.9±19.1)mg/d,化疗后(10.6±3.O)mg/d(P<0.01),2例已经脱离激素治疗。7例患者化疗前重度贫血,1例中度贫血,血红蛋白浓度为(52.8±13.6)g/L,化疗后2例进步,6例明显进步,血红蛋白浓度为(85.5±17.1)g/L(P<0.01)。8例患者中除1例从未输过血外,6例患者化疗后完全脱离输血;另1例输血间期延长。提示DA或HA方案化疗能够有效地减少PNH克隆负荷,控制溶血,改善血常规,而且大大减少了激素的用量,无严重、致命的不良反应。
异基因造血干细胞移植
这是目前唯一能够治愈PNH的方法。BMT治疗一般仅限于那些难治性、耐肾上腺皮质激素或有激素禁忌症的PNH患者。移植前要进行化疗,只有在预处理中尽可能地清除PNH克隆,才能够防止PNH复发。对于大多数患者目前还是以药物治疗为主。
抗凝治疗
静脉血栓是PNH最重要的并发症,主要在腔静脉和颅静脉,约50%的欧美PNH患者发生过静脉血栓,且约1/3由于血栓致死。东方人较西方人更易罹患再生障碍贫血,PNH患者也以PNH/AA综合征表现多,溶血和血栓的表现要少些。PNH患者易形成血栓确切原因未知,但目前已知道GPI缺乏的血小板较正常血小板更易被补体激活。
由于一次静脉血栓发生就可以对PNH患者的预后产生极大影响,已有建议在PNH患者中常规抗凝治疗。回顾性研究分析表明,华法令能显著降低血栓的形成,建议中性粒细胞中PNH克隆超过50%,血小板大于10万/dL,无其他华法令禁忌症者考虑使用。关于抗血小板药物,如阿司匹林的应用尚无研究报道。
总之,流式细胞技术在PNH的诊断中发挥着重要作用,只采用抗CD55和CD59抗体对红系和粒系检测的方法相对已较成熟,但对于那些只有粒系表达障碍的患者此种检验方法就存在局限性。FLAER为基础的多参数分析弥补了这一不足,但目前还没有统一诊断标准。在治疗上主要是Eulizumab所引起的不良反应,常见的有头痛、背痛、乏力、上呼吸道感染、单纯性疱疹、便秘等。应用Eulizumab的病人会出现脑膜炎球菌感染,因此在开始治疗前2周要注射脑膜炎球菌疫苗。此外,在临床应用过程中尚存在限制因素包括:①药物相关因素:Eculizumab可显著减少血管内溶血,但并不能治愈PNH,患者一旦应用Eculizumab,则需每两周输注一次直到患者去世或PNH自发消失(极少发生),若中断治疗,患者随即出现溶血性PNH临床症状及其并发症;输注次数频繁,输注计划严格,长期应用不良反应不可预知和价格昂贵等。至于其对PH的影响,由于病例数有限,Eulizumab是否真的能够逆转PH还需要大量的临床数据来证实。
小儿阵发性睡眠性血红蛋白尿症中医治疗
当前疾病暂无相关疗法。
日常保健
平时注意补充体内缺乏的营养,每天需要有足够的营养摄入体内。
一般预防
引起造血干细胞发生获得性基因突变的确切病因目前尚不清楚,感染,特别是病毒感染,药物(如阿司匹林,氯丙嗪,氯化铵,呋喃坦啶,铁剂等),输血,手术,劳累,精神创伤等均可诱发溶血,因此,防治上述诱因有利于预防疾病的发作。
1.血象 多为正细胞正色素性贫血,如合并缺铁则呈小细胞低色素性贫血,网织红细胞常增高,有时减低;白细胞数常减少,合并感染时常升高,血小板常减少。
2.骨髓象和骨髓培养 不同患者或同一患者在不同的病期中其骨髓象可有不同,多数病人的骨髓增生活跃,以中幼红细胞和晚幼红细胞增生为主,多见于血红蛋白尿发作者;少数病人的骨髓增生减低或重度减低,多见于血红蛋白尿不发作者,骨髓铁染色常阴性,但经多次输血或骨髓增生低下者,其骨髓铁正常或增多,骨髓培养常可发现CFU-E和CFU-GM等的集落数少于正常。
3.尿检查 可见血红蛋白尿,潜血试验阳性,含铁血黄素(Rous试验)试验阳性。
4.特殊溶血试验
(1)酸溶血试验(Ham试验):其原理是:PNH异常红细胞在酸化血清后(pH为6.2),易被补体旁路激活的补体攻击而破裂,此试验有较强特异性,阳性是诊断本病的重要依据,该试验的敏感性取决于血清中镁离子的浓度,如果血清中镁离子浓度调升到5mmol/L,则可提高该实验的敏感性,但是,该试验难以检测到小的异常细胞群和对补体中度敏感的红细胞。
(2)蔗糖溶血试验:这是一种简便的筛选试验,其原理是在离子浓度低的蔗糖溶液中,补体血清与红细胞膜的结合加强,造成红细胞膜的缺损,使红细胞内的血红蛋白溢出而溶血,本试验比酸溶血试验敏感,但特异性较差,如在巨幼红细胞性贫血,免疫性溶血性贫血和粒细胞白血病等均可出现阳性。
(3)蛇毒因子溶血试验:本实验也有较强的特异性,敏感性较Ham强,比糖水溶血实验略差,其原理是从眼镜蛇提取出的一种蛇毒因子(本身没有溶血)在血清的协同下通过激活补体旁路使PNH异常红细胞破裂而溶血,正常红细胞则否。
(4)补体溶血敏感试验:通过观察使抗体致敏红细胞发生溶血所需要的补体量,可以判断异常红细胞的比例及其对补体溶血的敏感程度。
5.GPI连接蛋白检测 一般情况下,可用相应的单克隆抗体结合流式细胞仪分析检测血细胞CD55和CD59的表达,该试验有在粒细胞和血小板易于操作的优点;而且这两种细胞群中的异常细胞所占比例大于红细胞中的异常细胞所占比例,这与血循环中异常粒细胞和血小板的寿命正常有关,一般而言,CD59缺乏最常见,CD16α缺乏最少见,目前认为,检测粒细胞或红细胞上GPI连接蛋白敏感性高,特异性强,结果可靠, 常规做影像学检查,如胸片,B超,注意有无肺部感染,胆石和肝,脾肿大等,血管造影可发现静脉血栓,脑CT检查可发现脑血栓。
由于长期溶血,可致胆石症,本病的血小板膜与血浆补体的相互作用失常,导致血液高凝状态而引起血栓形成,以下肢静脉和肠系膜静脉的血栓形成较为多见,腹部静脉栓塞时出现类似急腹症的剧烈腹痛,若门静脉栓塞,可引起门脉高压甚至肝功能衰竭,长期血红蛋白尿可引起肾内含铁血黄素沉着,而致含铁血黄素尿,长期的血红蛋白尿和含铁血黄素尿又可使体内铁丢失,而致缺铁性贫血,由于血小板减少及其功能异常,而有出血倾向,由于长期红细胞破坏过多或输血过多可致黄疸或皮肤色素沉着,肝脾肿大,有些可出现再生障碍性贫血的临床表现,少数病人可转变为急性白血病或骨髓纤维化。