恶性组织细胞病(恶组)是单核—巨噬细胞系统中组织细胞的恶性增生性疾病,临床表现以发热,肝脾淋巴结肿大,全血细胞减少和进行性衰竭为特征。恶组多见于青壮年,以20~40岁者居多,男女发病为2~3:1。本病按病程可分为急性和慢性型。国内以急性型为多见,起病急骤,病情凶险且病程较短,未经化学治疗者大多数病例在起病6个月内因消耗衰竭,肝肾功能衰竭、胃肠道及颅内出血而死亡。由于症状,体征及实验室检查无特异性,目前国内诊断本病仍主要依靠临床表现,骨髓细胞形态及(或)活体组织病理学检查。早期诊断较困难。
-
挂什么科:内科 血液科
-
需做检查:皮疹 大生化检查 碱性磷酸酶染色 胸部平片 骨髓象分析 苏丹黑B染色 血沉方程K值 免疫病理检查 CT检查
-
治疗方法:药物治疗 支持性治疗
-
常用药物:暂无相关信息
-
一般费用:根据不同医院,收费标准不一致,市三甲医院约(80000——90000元)
-
传染性:无传染性
-
治愈周期:1-3个月
-
治愈率:70%
-
患病比例:0.003%
-
好发人群:多见于青壮年,以20~40岁者居多,男女发病为2~3:1
-
相关症状:
-
相关疾病:
根据恶组细胞浸润部位的不同,临床上可有不同的表现,从上述病理累及部位来看可累及造血组织(最常见),又可累及非造血组织,因此临床表现多种多样,国内作者曾提出不少分型意见,如按Israels分为5型,实则多数恶组病理,临床表现具有2型以上的特点,虽然Cazal将其简化为内脏型,皮肤型,儿童型,但认为儿童与成人临床差异不大,有提出病变主要累及造血组织称普通型,主要累及非造血组织则称特殊型,有关特殊型提法更多,如,皮肤型,胃肠型,肺型,肾型,神经型,多发性浆膜炎型,肠穿孔型,巨脾及脾自发破裂型,慢性复发型,等等,也有作者认为临床表现多样,难以某型概括,临床与病理对照也不尽一致,认为分型对预后意义不大,对待分型国内目前尚无统一意见,此外,有提出根据病程分急性和慢性(1年以上为慢性),由于慢性很少见,大多数病例发病急,病程短,故临床上未强调急,慢之分,1975年在福建三明市召开的恶组座谈会上对慢性型未作定论,现将国内文献报道(包括特殊类型)的862例综合分析如下,以了解临床表现的多样性。
1.首发症状
不论是何种类型的恶组,发热常是首发表现,热型以不规则高热居多(38.7%),其次为稽留热(26.3%),弛张热(21.2%),间歇热(10.8%)及低热(3%)少见,苍白,乏力是因贫血所致,出血倾向在首发表现中亦不少见,尤其到病程晚期愈来愈重是致死原因之一,黄疸一般在早期常不明显多在较晚期出现,但也有部分患者以黄疸首发而住入传染病医院,此外,国内报道不少例以发热,腹痛及反复血便首发,因常伴有肠穿孔而误为急腹症入外科手术探查,再有恶组侵犯肺部而误为肺炎,肺部肿瘤,肺结核的报道亦不断涌现,另有以截瘫,脑神经麻痹或颅内压增高为首发表现者有不少个案报道,值得提出的有的患者骨,关节痛常很显著,止痛药物常无效。
本病按病程可分为急性和慢性型。
(1)发热是最为突出的表现,90%以上病人以发热为首发症状,体温可高达40°C以上,热型以不规则热为多,也有间歇热,弛张热和稽留热,少数病例用抗生素能暂时使体温下降,但更多病例发热与疾病本身有关,对抗生素治疗无反应,皮质激素虽有降温作用,但不持久,只有化疗有效时体温才能恢复正常。
(2)贫血也是较常见症状之一,急性型早期即出现贫血,呈进行性加重,晚期病例,面色苍白和全身衰竭非常显著,少数起病缓慢的病例,其最早出现的突出症状可为贫血和乏力。
(3)出血以皮肤瘀点或瘀斑为多见,其次为鼻衄,齿龈出血,粘膜血疱,尿血,呕血或便血也可发生。
(4)此外,乏力,食欲减退,消瘦,衰弱也随病情进展而显著。
2.体征
肝大,脾大是常见的体征,常呈轻度或中度肿大,1例肝最大在右肋下10cm;1例脾最大入盆腔,但在胃肠型恶组约1/3病例肝,脾未触及,2/3肿大者为轻度肿大,表浅淋巴结一般似黄豆大,花生米大,最大如鸡蛋大,从尸检情况看,恶组主要侵犯深部淋巴结,浅表淋巴结不大并不能排除恶组,皮肤损害以结节和肿块最为常见(可形成肉芽肿或导致纤维化,肉眼上形成结节,但镜下细胞彼此并不黏聚),并可伴有溃疡,尚可伴有非特异性损害,如斑丘疹,紫癜及红皮病等,皮肤损害在儿童恶组中较为多见,并被认为是其特征,肺部可有啰音伴有咳嗽,气短,腹部触及肿块者多为肠型恶组之体征,有人统计53例以肠道症状首发者(除发热,腹痛,腹泻外),腹部触及肿块占41.5%,而发生肠穿孔者高达52.8%。
(一)发病原因
目前尚不清楚,通常认为是组织细胞性淋巴瘤或急性单核细胞性白血病的一种变型,可能与EB 病毒感染有关,亦有人士认为是自身免疫增殖性疾病或者由于免疫功能缺陷所致,近年来报道恶组常作为继发于其他肿瘤的第2个恶性肿瘤,常伴发于恶性淋巴瘤(B 细胞性),T 细胞性和裸细胞性急性淋巴细胞性白血病,急性粒—单核细胞白血病, Lennerts 淋巴瘤,推测可能于化疗或原发肿瘤抑制免疫系统,导致染色体异常,克隆恶性突变有关,本病的发生可能与患者的免疫功能低下有关,由于尸检中部分病例有肥大细胞增生现象有人认为是一种自身免疫增殖性病变,初为过敏,渐转化为肿瘤,有人注意到恶组患者血清EB病毒抗体效价增高,怀疑本病与病毒感染有关,已知EB病毒是引起Burkitt淋巴瘤的病因,但在恶组病因中起何作用尚不清楚,有人注意到近年来恶组在中非地区发病率有所上升,推测可能与环境因素特别是与病毒因素有关,但目前尚缺乏有力的血清学和流行病学证据,Kobari等观察到1例慢性EBV感染病人后发生恶组,通过PCR法扩增,EBV定位于淋巴细胞膜的抗原,用原位杂交法(ISH)检测DNA中的EBV,结果发现早期慢性感染时非恶性的组织细胞中存在的EBV颗粒与后来的恶组细胞中的EBV颗粒相同,由此推论可能原本正常的组织细胞受EBV感染后变成异常细胞,并发生克隆性扩增,结果产生恶组,国内梁平(1984)对8例恶组骨髓标本做电镜观察,在2例恶组细胞内见到Ⅳ型核小体,认为它是细胞曾受病毒作用的一个形态学标志,国外有人怀疑本病与遗传因素有关,有父子先后发病的报道,国内关敏等(1990)报道有2例为同胞兄弟,且其家系中另有1兄弟患病,3兄弟均在婴幼儿时期发病,病情相同且均在发病后3个月内死亡,近年来国内学者发现恶组尸检中全身淋巴组织呈现重度萎缩,推测患者伴有免疫功能缺陷,至于免疫缺陷是病因还是结果尚无定论,总之,病因至今仍不明确。
(二)发病机制
目前不明,1969年Rodman报道了2例恶组有染色体易位,即t(2;5)(p23;q35),此外尚有1号染色体异常,Morgan等在1986年发现恶组细胞株中5号染色体长臂一固定点的断裂(5q35断裂),并常伴有t(2;5),另有报道1号,3号和6号染色体也有易位,Morris(1994)等证实t(2;5)可产生NPM/ALK融合基因,Shiota等(1995)指出,此融合基因编码一个(80kD)的高磷酸化蛋白(p80),NPM/ALK融合基因和p80见于所有t(2;5)的病例中,但能表达p80 NPM/ALK者是一个独立的病种,通过细胞遗传学或p80表达的测定,5q35断裂目前可作为诊断CD30阳性肿瘤的前提,国内吴士琪等(1983)提出D组染色体丢失1条是本病较常见的核型,1989年Stephen等报道了3例“恶组”,均表达ki-1(CD30),皆有t(2;5)(p23;q35)易位,认为这种易位可能是具有恶组特点的一组病共有的特征,1990年Abe等研究了4例恶组的细胞遗传学,其中2例有17号染色体异常,断点在短臂13(17p13),复习文献另有7例恶组亦有相同异常发现,现已有证明p53基因突变在人类恶性肿瘤的发生率较高,而p53(抑癌基因)即定位于17号染色体短臂,1992年国内田虹等对2例恶组白血病型患者进行骨髓染色体分析,均出现1号部分三体(1qter-1p11)和1p11断裂易位。
诊断
过去诊断本病主要仍依靠临床表现和细胞形态学或活体组织病理检查结果,近年来对本病的恶性细胞来源有了新的认识,甚至提出应当更改病名,但作为同一 个疾病实体,它的临床表现和细胞,病理形态所见与过去的描述不应有差别,因而过去的诊断依据仍沿用,只是需要增加一些细胞标志,细胞和分子遗传学方面的指 标以确定恶性细胞的来源,以便准确地对疾病命名。
1.临床表现
以发病急,长期发热,伴进行性肝脾淋巴结肿大,进行性肝肾功能衰竭,进行性全血细胞减少,进行性全身衰竭为特点,常伴黄疸,出血,可有皮肤损害和浆膜腔积液。
2.骨髓涂片
确诊必须找到一定数量的上述的异常细胞,由于骨髓不一定经常受累,且病变常呈灶性分布,因此骨髓1~2次检查阴性不能除外本病,需多次重复检查,国内有人 提出胸骨穿刺阳性率高于髂骨(4例髂骨阴性改作胸骨穿刺均呈阳性,又有数例髂骨穿刺涂片异常细胞只占1%,换作胸骨穿刺则异常细胞占有核细胞的8%)。
3.外周血浓缩涂片检查
统计305例外周血涂片有152例(49.8%)找到异常细胞,血液浓集后找到异常细胞的机会更高些,血液浓缩涂片可与骨髓涂片相互补充参照。 目前主要诊断恶组的方法是依靠骨髓穿刺涂片检查,骨髓1次确诊的成功率为69%,骨髓找到“恶组”细胞占有核细胞的2%~78%(其中占2%~20%为 77.1%,占72%以上为22.9%),有人提出通过5次的骨髓穿刺,98%的病例可以诊断,实际上生前未能确诊的仍有10.2%患者,而另有 10.3%患者需依靠其他部位的活组织采取病理检查(表4),关于其他部位活组织采取确诊的成功率:皮肤活检72.7%(24/33);淋巴结活检 63.1%(70/111);骨髓活检39.7%(27/68);肝脏活检25%(5/25),此外有个别作淋巴结穿刺,脾穿刺,心包穿刺,肺穿刺,脑脊 液及胸腹水找到“恶组”细胞,浅表淋巴结活检成功率低于皮肤活检是由于“恶组”多侵犯深部淋巴结,而骨髓活检及肝活检只能做辅助诊断是由于“恶组”常呈灶性浸润,穿刺不易抓到。
总之,关于诊断必须强调临床表现的重要性,国内不少学者同意作者(1973)的观点,即临床怀疑本病又有形态学支持则可初步诊断;临床怀疑而无形态 学变化不能排除本病,应反复进行多部位骨髓穿刺(胸骨穿刺阳性率可能较高)及可能的活组织病理检查;有形态学特点但与临床表现不符者,需与反应性及其他组织细胞增生性 疾病相鉴别,为确定恶性细胞来源,应作多种细胞化学,免疫标志以及细胞和分子遗传学检查,Ki-30(CD30)阳性,t(2:5)(p23:q35)染 色体移位,有融合基因NPM/ALK(p80)者,有助于确定为间变性大细胞淋巴瘤,其他标记物如上皮膜抗原(epithelial membrane antigen, EMA)和CD25(IL-2受体)也可能阳性。
鉴别诊断
恶性组织细胞病应与反应性组织细胞增多症,急性白血病,骨髓转移癌,再生障碍性贫血等疾病鉴别。
本病的临床表现多种多样且无特异性,因此单根据临床表现极易发生误诊,综合国内报道的669例初诊误诊率高达69.4%,国内文献报道的误诊病种多达70多种,常易误诊的情况:
①因发热,出血,全血细胞减少而诊为再生障碍性贫血,急性白血病等;
②因发热,黄疸,肝脾大而误诊为黄疸性肝炎,肝硬化,胆道感染等;
③因发热持续不退伴有胃肠道症状而误为伤寒,败血症,肠结核等;
④因便血,腹泻或腹部肿块而考虑为肠道肿瘤,淋巴瘤,溃疡性结肠炎等;
⑤因发热,咳嗽,气短,胸液而误为肺部感染,肺肿瘤,肺结核等;
⑥因发热,血尿,水肿而诊为肾小球肾炎,泌尿系感染,甚至尿毒症;
⑦因发热伴截瘫,脑神经麻痹或抽搐而误为脑炎,脊髓炎,颅内肿瘤;
⑧因发热伴有心包积液或胸腹腔积液而误为多发性浆膜炎;
⑨因鼻咽部溃疡而误为坏死性肉芽肿;
⑩因发热,皮肤结节溃疡或红斑而误为皮肤结核,非化脓性脂膜炎,蕈样霉菌病等,此外,有不少病例误为外科疾病而施行手术探察,故应提高对本病的警惕。
有骨髓的细胞形态学的支持,可以帮助诊断,但是许多非肿瘤性疾病也可引起反应性组织细胞增多,常与本病鉴别。
1.反应性组织细胞增生的概念
是指有明显的原发病存在,由于原发病的某些因素的刺激而发生组织细胞增生,待原发病去除,刺激减轻后增生的组织细胞可自然消失,当原发病诊断明确而组织细胞反应性增生程度较轻时,后者易被忽视,但若重症患者,其组织细胞反应强烈,而原发病诊断不明时易误诊为“恶组”,已知某些感染性疾病如结核病,伤寒,布氏杆菌病,疟疾等可引起骨髓组织细胞增多,并有吞噬血细胞现象,过去对组织细胞增生的概念及分类比较混乱,20世纪70年代提出将反应性组织细胞增生分为3类:
①感染性:继发于感染性疾病,包括上述疾病及肝炎,传染性单细胞增多症等;
②变态反应性:继发于结缔组织病,药物过敏,皮炎性淋巴结病及某些疫苗接种反应;
③恶性肿瘤性疾病:在未转移到骨髓时亦可有组织细胞增生。
20世纪70年代初张之南等通过随访工作,发现原诊断为恶组的部分病例,经过数年之后仍存活,有的发展为典型的类风湿性关节炎;有的以后查出为红斑狼疮;有的发现为迁延型肝炎;有的无任何疾病迹象,重新复习这些病例,过去的临床表现及骨髓细胞形态,结果:临床上发病很像“恶组”,有高热,苍白,肝脾大,全血细胞减少,个别有出血倾向,其中1例当时血压已下降至80/57mmHg,自动出院,大多病情十分凶险,但骨髓细胞形态大都是单核样和淋巴样细胞,个别有异型细胞,但为数不多(不超过1%),仅有1例数量较多(约20%),血压下降自动出院,当时并无关节症状,多年后关节明显畸形变形,实为类风湿性关节炎,由此可见,个别反应性组织细胞增生与“恶组”在初期较难鉴别。
1979年Risdal等报道19例因病毒感染引起组织细胞增生并有吞噬血细胞现象,其中14例发病前曾接受较长时间的免疫抑制剂治疗,病毒检查阳性,称之为病毒相关噬血细胞综合征(virus-associated hemophagocytic syndrome,VAHS),其后发现不仅病毒可引起噬血综合征,很多细菌,真菌,甚至近期输血,肿瘤播散等也可引起,有称感染相关性噬血细胞综合征(infection-associated hemophagocytic syndrome),有称噬血细胞性组织细胞增生症(hematophagic histiocytosis),此外有称噬血细胞综合征(hematophagic syndrome)者,都是从骨髓细胞学角度提出的,表现为组织细胞增生并活跃地吞噬各种血细胞。
已查明许多病原体可引起噬血细胞综合征:
①病毒,如EB病毒,巨细胞病毒,单纯性疱疹病毒,水痘带状疱疹病毒,腺病毒,微小病毒B19;
②细菌,如肠道革兰阴性杆菌,流感噬血杆菌,肺炎双球菌链球菌,金黄色葡萄球菌,流产布氏杆菌,肺炎支原体等;
③伯纳特立克次体;
④结核分枝杆菌;
⑤真菌,如荚膜组织胞浆菌,白色念珠菌,新型隐球菌。
⑥利什曼原虫,噬血细胞综合征的临床表现随原发病的不同而不一,最常见的共同症状为发热,以高热居多,可伴有寒战,盗汗,纳差,体重减轻及肝,脾,淋巴结轻度肿大,部分患者可有出血,皮疹,全血细胞减少,肝功能损害或凝血功能障碍,VAHS尚可有中枢神经系统症状,肺部浸润或肾功能衰竭等多脏器损害症状,VAHS常于病前2~6周有病毒感染症状,虽然噬血细胞综合征本质上属于一种反应性组织细胞增生,如无继发性感染多在l~8周内自然缓解,但在严重病例,其临床过程极似“恶组”,死亡率可高达30%~40%,病情凶险程度几乎难于与“恶组”相区别,如Chen等1991年报道10例台湾儿童由EB病毒引起的爆发性VAHS,临床表现有发热,黄疸,肝脾肿大,全血细胞减少,凝血障碍和肝功能异常,骨髓检查有非典型T淋巴样细胞及少数B免疫母细胞浸润,并有成熟组织细胞增生伴吞噬血细胞现象,最初6例曾诊断为恶组,10例均迅速死亡,从发热到死亡平均生存期为16天,主要死因为凝血功能障碍伴多脏器衰竭和机会致病菌感染,应用血清学鉴定和印迹杂交实验证实为EB病毒急性感染。
2.反应性组织细胞增生的实验室检查
(1)外周血细胞有不同程度减少:国内82例反应性组织细胞增生症就诊时已有贫血者占48.4%;全血细胞减少者占14.6%;其余为血小板减少或白细胞减少或三系中2系减少,少数为白细胞增高(7.3%);外周血涂片见到成熟组织细胞者占17.8%(1%~31%),国外资料中有贫血,白细胞及血小板减少者分别为9l%,80%和88%。
(2)骨髓涂片可见组织细胞增多:细胞大都是成熟型或单核样及淋巴样组织细胞,可伴有血细胞被吞噬,个别病例可见少量异常组织细胞或可见到1~2个多核巨细胞,目前认为全血细胞减少不都是组织细胞吞噬血细胞过多所致,而是感染抑制骨髓的结果。
(3)其他实验室检查:常有血清谷丙转氨酶升高,可有氮质血症,或血胆红素增加,凝血酶原时间延长,低丙种球蛋白血症,血α2球蛋白比例增高,乳酸脱氢酶升高等,VAHS患者血清中病毒抗体滴度可升高,病毒培养可阳性,其他原因的反应性组织细胞增生,可迟早出现原发病的征象及相应的实验检查所见。
3.恶组与反应性组织细胞增生症的鉴别
1994年冯云等报道1986~1992年确诊的噬血细胞综合征与“恶组”病各13例的异同。
可以看出,从临床表现及细胞形态区别有时确有困难,而病原学检查及血清铁蛋白检测对二者鉴别可能有帮助,有认为血清铁蛋白在“恶组”明显高于反应性组织细胞增生症,但亦有报道两病的血清铁蛋白均显著增高,二者并无显著差异,此外,中性粒细胞的碱性磷酸酶(NAP)在“恶组”的阳性率和积分极低,而反应性NAP大多数增高,有认为“恶组”细胞分化差有较多的核分裂象,吞噬血细胞现象较少见,而反应性组织细胞分化较成熟,很少出现分裂象,而吞噬血细胞现象极为明显,我们过去的经验表明:在没有合并明显感染的情况下,可试用肾上腺皮质激素,反应性者用药2~3天体温可渐退并可在短期内停药,虽然有少数患者可再发热,但可有较长间隔,再用药体温仍可退,需视原发病是否已同时治疗而定,我们曾对38例反应性组织细胞增生症进行分析,其中16例原发病不能确定,9例未经特殊治疗体温自然下降,7例口服泼尼松后热退,热退后肝脾及淋巴结缩小,血象及骨髓象逐渐恢复正常,而恶组对肾上腺皮质激素反应差,即使体温有下降,常不能降至正常或下降后短期又上升,且连续应用逐渐失效,有报道有些噬血细胞综合征应用环孢素A(cyclosporin A)有效,需强调的是,骨髓发现有吞噬现象的组织细胞增多应首先排除反应性者,因为多见,约有半数以上的反应性者较易找到原发病,一般反应性组织细胞增多持续时间不长,多次重复骨髓穿刺检查变化较大,消失较快,而恶组一旦骨髓出现异常组织细胞后,重复骨髓穿刺异常细胞会逐渐增多。
恶性组织细胞病西医治疗
(一)治疗
目前尚缺乏有效的治疗方法,现采用的主要措施是抗癌药物的联合化疗。郁知非等报道用米托蒽醌加环磷酰胺、洛莫司汀(环己亚硝脲)、长春新碱和泼尼松联合化疗恶组数例,多数病人获得完全缓解例已无病生存分别达10年和10年以上。1990年Sonneveld等报道12例恶组,4例治疗前死亡(生存期8天~2个月);6例用CHOP方案(环磷酰胺、柔红霉素、长春新碱、泼尼松)2例并做了脾切除,经多个疗程后,结果4例分别存活>11个月、>30个月、>83个月、>85个月。国内谢丽蓉等(1983)对1例有巨脾者行脾切除,术后采用CHOP方案,病情相对稳定,提出巨脾切除可纠正脾功能亢进,除去大部分的肿瘤病灶,有利于化疗的进行。1993年姚达明报道以CHOP方案治疗5例恶组,3例完全缓解,其中1例已存活1年。此外,已有报道用同种异体骨髓移植治疗恶组成功的病例。这些治疗方法与近年来国外采用的治疗方案都与治疗非霍奇金淋巴瘤的化疗方案相近。
一、支持治疗
包括降温治疗,采用物理措施降温,必要时适当应用皮质激素;注意预防和治疗继发感染;患者往往有高热、大汗,注意水电介质平衡;纠正贫血,可输新鲜全血或充氧血;预防出血,血小板过低可输注血小板悬液。
二、化疗
不管应用单药化疗或联合化疗,效果均不满意,难以得到持久的完全缓解。一般可采用治疗恶性淋巴瘤或治疗急性白血病的化疗方案治疗,少数缓解期可达6-12个月。
重症病例病程进展快。末经治疗的自然病程为三个。轻型起病缓,进展慢,未经治疗可存活1年以上。对治疗有反应者,获得缓解的病人,生存期可延长。
1.国内疗效标准
(1)完全缓解:症状及属于本病的不正常体征均消失。血红蛋白浓度≥100g/L,白细胞数≥4.0×109/L,分类正常,血小板数≥100×109/L;骨髓涂片中找不到异常组织细胞。
(2)部分缓解:自觉症状基本消失,体温下降或稳定一段时间,肿大的肝、脾、淋巴结明显缩小(肝、脾最大不超过肋缘下1.5厘米)。血象接近但未达到完全缓解标准。骨髓液涂片中异常组织细胞基本消失或极少量。
2.国外疗效标准
根据Zucker及Tseng报道的资料综合如下。
(1)完全缓解:症状及体征消失,未在新的部位出现肿瘤性病变,骨髓涂片中未见恶性细胞。
(2)部分缓解:可供测定的病灶和肿大的组织器官的最大垂直直径减少≥50%,且不出现新的病灶。
(二)预后
本病大多发病急、病程短。Ishii等报道在14例恶组病人中,血清TNF浓度≥50pg/ml者病情严重,预后极差。而凝血状态和血清LDH、铁蛋白和IL-1的血清浓度与预后无关。综合国内报道病例808例,观察到死亡者669例,87.1%生存期<6个月;7.9%生存期为6个月~1年;仅有5%生存期>1年以上(最长1例14年)。在作者综合的1458例中有8例发生白血病(0.55%)。“恶组”死亡原因最多见为全身衰竭;其次为出血(主要是胃肠道,其次为颅内);再次为严重感染;少数由于肝肾功能衰竭或心力衰竭致死。单纯累及皮肤而无内脏器官侵犯者预后较佳,可存活10多年。侵犯内脏的病例,预后都很差,与年龄、性别、侵犯部位等因素无关。
恶性组织细胞病中医治疗
当前疾病暂无相关疗法。
1)维持理想的体重。
2)摄入多种食物。
3)每天饮食中包括多种蔬菜和是水果。
4)摄取更多的高纤维食物(如全谷麦片、豆类、蔬菜、水果)。
5)减少脂肪总摄入量。
6)限制酒精类饮料的摄取。
7)限制腌制、熏制、及含亚硝酸盐类食品的摄入。
1.协助病人日常生活,降低耗氧量,减轻心,肺负担。
2.保证病人充足的休息和睡眠时间,保持环境安静,舒适,避免不必要的操作,减少干扰因素,如噪音,探视者,注意保暖,避免受凉。
3.经常与病人一起讨论能够预防或减轻疲劳的方法,如尽量避免诱发因素,保持病情稳定,降温,止痛,及时更换汗湿衣裤,被服。
实验室检查 1.外周血
患者就诊时血象正常者仅约10%,其余均有各种血细胞不同程度的减少(少数病例白细胞计数可增高),随着病情的发展全血细胞减少愈趋明显,成为本病的突出表现之一,约有半数患者在外周血片末端边缘易找到异常细胞(特别是用浓缩法或在白细胞层)。
2.骨髓象
在骨髓涂片中多数仍可见到各系正常造血组织,分析241例骨髓涂片,有66.4%骨髓呈活跃或明显活跃;33.6%呈增生减低或重度减低,由于病变呈灶性分布很不均匀,有时多次骨髓穿刺均未能找到恶性细胞,当各种恶性细胞混杂在骨髓涂片中出现时,可呈大小不等及多形性,细胞学形态的变化国内外描述并非尽同,1964年全国血液学术会议上,根据细胞形态特点,分成下列类型:
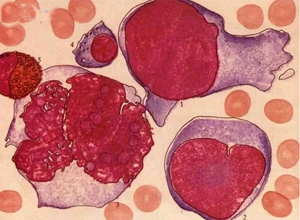
(1)异常“组织”细胞(恶性“组织”细胞):体积较大(20~40μm)外形规则或呈不规则圆形,胞质比一般原始细胞丰富,胞质深蓝或浅蓝色,深蓝者常无颗粒,浅蓝者可有少数或较多细小颗粒,可有数量不一的空泡,核可呈圆形或椭圆形,有时呈分枝状,偶有双核者,核染色质细致或呈网状,核仁显隐不一。
(2)淋巴样“组织”细胞:如淋巴细胞大小,外形和淋巴细胞或内皮细胞相似,可呈椭圆形,不规则圆形或狭长带有弯曲的尾巴,胞质呈浅蓝色,灰蓝色,含有较多细小颗粒,核常偏于一侧或一端,核染色质较细致,偶见核仁。
(3)单核样“组织”细胞:形态颇似单核细胞,但核染色较深或粗颗粒较明显。
(4)多核巨细胞:体积甚大,直径可达50μm以上,外形不规则,胞质浅蓝无颗粒或有少数细小颗粒,通常含有3~6个核或核成分叶状,核仁或隐或显。
(5)吞噬细胞:体积可以很大,单核或双核,椭圆形偏位,染色质疏松,核仁清晰,胞质中含有被吞噬的成熟红细胞或其碎片,幼红细胞,血小板及中性粒细胞等,一个吞噬细胞最多可吞噬20余个血细胞。
据我们观察,认为异常“组织”细胞及(或)多核“组织”细胞有特异性诊断价值,而淋巴样和单核样细胞在其他疾病中也可出现,无特异性诊断意义,至于骨髓涂片中有多少异常的“组织”细胞即可诊断,一直无明确规定,1959年郁知非等报道的18例,骨髓异常“组织”占有核细胞的10.5%,最多达88%。
3.组织化学染色
本病特殊细胞的细胞化学反应多表现为过氧化物酶染色阴性,苏丹黑染色阴性或弱阳性,糖原染色多为弱阳性弥散反应;酸性磷酸酶染色多为中等度强阳性反应能被酒石酸抑制,葡萄糖醛酸酶染色弱阳性~中等阳性反应;非特异性酯酶染色阳性~强阳性反应,能被氟化钠抑制;α-ASD氯乙酸萘酯酶和碱性磷酸酶呈阴性反应,溶菌酶染色阳性,α1-抗胰糜蛋白酶和α1-抗胰蛋白酶阳性。
4.生化检查
有62%血清谷丙转氨酶增高;54.3%尿素氮增高;亦有部分病例乳酸脱氢酶,碱性磷酸酶升高,血清铁蛋白含量明显增高。
5.47.6%血沉增快,中性粒细胞碱性磷酸酶减低。 辅助检查
1.病理检查
淋巴结皮肤,肝脏,骨髓等病理活检找到恶组细胞。
2.X线
胸部X射线摄片多有改变,如:弥漫性或间质性浸润,散在的粟粒状及小结节状阴影,或纵隔肺门淋巴结肿大,胸腔积液等,但X射线表现一般为非特异性,而经常与并发症同时存在。
3.CT,MRI检查
发现头颅,腹部,肝,脾,腹膜后淋巴结及胸部等病变。
4.B超
肝脾淋巴结肿大,胸腔积液,腹水等。
本病的并发症有高热衰竭,出血和感染,严重者可导致死亡,恶组病变常累及多个脏器,尤其是急性型,起病急,病程短暂且凶险,可出现发热,贫血,出血,肝,脾,淋巴结肿大,咳嗽,胸痛,呼吸困难,腹痛,消化道出血等,这些即是它的临床表现,同是亦是它的并发症,在临床上很难加以区别。